معادله هامت
معادله هامت الگو:انگلیسی ، رابطهای در شیمیفیزیک آلی است که سرعت واکنش و ثابت تعادل در نوع مشخصی از واکنشهای آلی را به هم مرتبط میسازد.
لوییس هامت
مطالعات محققی به نام لوییس هامت (۱۸۹۴-۱۹۸۷) نشان داد که بین ویژگی های الکترونی اسیدها و بازهای آلی با ثابت های تعادل و واکنشپذیری آنها ارتباط مستقیمی وجود دارد.
تشریح معادله
معادله به صورت زیر است:
در اینجا K ثابت تعادل، K0 ثابت تعادل برای اتم هیدروژن (مرجع)، ρ ثابت واکنش و σ ثابت جانشینی است. در مواردی که گروه استخلافی ، ویژگی الکترونکشندگی دارد، مثل گروه نیترو، ثابت تعادل افزایش پیدا می کند و بسته به موقعیتی که این گروه جانشین شده روی حلقه آروماتیک انتخاب می کند - متا یا پارا - این اختلاف بیشتر می شود.
در موردی که گروه استخلافی الکتروندهنده مثل اتیل به حلقه آروماتیک متصل شده است ثابت تعادل کاهش پیدا کرده است.
استخلافهای گوناگون
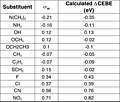
مقدار ثابت جانشینی برای گروههای استخلافی گوناگون:
| گروه جانشینشونده | اثر پارا | اثر متا |
|---|---|---|
| دیمتیلآمین | -۰٫۸۳ | -۰٫۲۱۱ |
| آمینو | -۰٫۶۶ | -۰٫۱۶۱ |
| متوکسی | -۰٫۲۶۸ | +۰٫۱۱۵ |
| اتوکسی | -۰٫۲۵ | +۰٫۰۱۵ |
| متیل | -۰٫۱۷۰ | -۰٫۰۶۹ |
| هیچیک | ۰٫۰۰۰ | ۰٫۰۰۰ |
| فلوئور | +۰٫۰۶۲ | +۰٫۳۳۷ |
| کلرو | +۰٫۲۲۷ | +۰٫۳۷۳ |
| برمو | +۰٫۲۳۲ | +۰٫۳۹۳ |
| یدو | +۰٫۲۷۶ | +۰٫۳۵۳ |
| سیانو | +۰٫۶۶ | +۰٫۵۶ |
| نیترو | +۰٫۷۷۸ | +۰٫۷۱۰ |